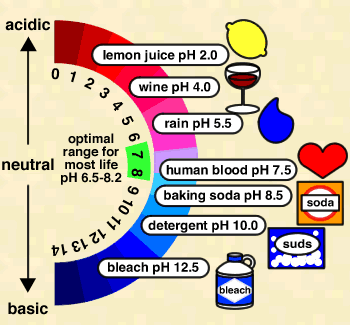
ในครั้งที่แล้วได้แนะนำเกี่ยวกับการตรวจวัดพีเอช ซึ่งบทความของเราได้รับการตอบรับอย่างล้นหลามจากทีมงานฝ่ายผลิต คราวนี้เราจะขอกล่าวย้อนไปถึงรายละเอียดของพีเอช หรือ potential of hydrogen ion ในเรื่องของความสัมพันธ์ของค่าพีเอชในเชิงปริมาณ
ในปี ค.ศ. 1887 Svante Arrhenius (อาเรเนียส) ได้ค้นพบและตั้งทฤษฎีว่า เกลือละลายน้ำ จะแตกตัวเป็น ไอออนบวก และไอออนลบ เค้าจึงเอาสิ่งที่ค้นพบมาสร้างความสัมพันธ์ และสร้างสถานะของทุกๆ สารละลายกรด ให้กรดแตกตัวออกเป็น H+ จากการค้นพบของ อาเรเนียส เขาจึงค้นพบว่าสภาพความเป็นกรดและด่าง จะขึ้นอยู่กับความเข้มข้นของ H+
จึงเป็น บทเรียนที่เราเรียนกันจนทุกวันนี้ คุ้นๆหูในนามของ นิยามกรด-เบส ของ อาเรเนียส ที่กล่าวไว้ว่า
กรด คือ สาร เมื่อละลายน้ำแล้วแตกตัวให้ H+
เบส คือ สาร เมื่อละลายน้ำแล้วแตกตัวให้ OH-
ค่า pH เป็นค่าที่ใช้บอกความแรงของกรดหรือเบสอย่างง่ายๆ นิยมใช้กันอย่างแพร่หลายกับผลิตภัณฑ์ทั่วไปไม่เฉพาะพวกสารเคมี คนทั่วไปเข้าใจได้ ค่าpHนี้กำหนดโดยความเข้มข้นของโปรตอน (H+) ในสารละลาย ยิ่งโปรตอนเข้มข้นมากซึ่งก็คือเป็นกรดมาก pHจะต่ำ ในทางกลับกันถ้าสารละลายเป็นเบส คือความเข้มข้นของโปรตอนต่ำ pH จะสูงค่าpH คำนวณได้จากสูตรนี้
pH = -log[H+]
โดย [H+] คือความเข้มข้นของโปรตอนในหน่วย โมล/ลิตร
โมล คือ หน่วยวัดปริมาตรทางเคมี โดยปกติอ้างอิงจากน้ำหนักจริงของสารหารด้วยน้ำหนักโมเลกุลของสารชนิดนั้น ซึ่งเป็นค่าคงที่
ในการวัดความเป็น กรด – เบส ในสารละลายนั้น เราใช้คำว่า “pH” เป็นตัวบ่งชี้ ตัว p ย่อมาจาคำว่า power ซึ่งมีความหมายในเชิงยกกำลัง ส่วน H นั้นหมายถึง ความเข้มของประจุไฮโดรเจน pH มีค่าเป็นตัวเลขตั้งแต่ 0 – 14 สารประกอบที่มีค่า pH 5 มีประจุไฮโดรเจนมากกว่า สารประกอบที่มีค่า pH 6 ถึง 10 เท่า
น้ำบริสุทธิ์มีค่า pH เป็นกลางอยู่ที่ pH 7 นั้นหมายถึง น้ำ 1 ลิตร ที่อุณหภูมิ 25 องศาเซลเซียส มีประจุไฮโดรเจน และประจุไฮดรอกไซด์ อยู่จำนวนเท่ากันคือ 1 x 10 –7 โมล
* เบสแก่ คือ เบสที่แตกตัวได้มากหรือ เบสที่แตกตัวได้ 100 % หรือเรียกอีกชื่อหนึ่งว่า
อิเล็กโทรไลต์แก่ ได้แก่ เบสหมู่ 1 ทุกตัว และเบสหมู่ 2 ยกเว้น Be(OH)2
* กรดแก่ คือ กรดที่แตกตัวได้มากหรือ เบสที่แตกตัวได้ 100 % หรือเรียกอีกชื่อหนึ่งว่า
อิเล็กโทรไลต์แก่ แบ่งออกเป็น
กรด Hydro ได้แก่ HCl , HBr , HI
กรด Oxy ได้แก่ H2SO4 , HNO3 , HClO3 , HClO4
ข้อสังเกต กรด Oxy ที่แก่ ให้นำจำนวนออกซิเจนลบกับจำนวน H+ ที่แตกตัวได้
ถ้าผลลัพธ์ตั้งแต่ 2 ขึ้นไปจะเป็นกรดแก่
ค่า pH ปกติมีค่าที่นิยมใช้กันคือ อยู่ระหว่า 0 - 14
โดยการวัดค่า pH นั้นที่ 0 วัดจากค่าความเข้มข้นของกรด HCl ที่ความเข้มข้น ที่ 1 M
pH ที่ 7 วัดจากค่าของน้ำ (Pure Water)
pH ที่ 14 วัดจากค่าความเข้มข้นของเบส NaOH ที่ความเข้มข้นที่ 1 M
ในกรณีที่เราต้องการค่า pH เป็น -1 ก็ทำการเตรียมกรดที่ 10 M แต่ถ้าต้องการวัดค่า pH ที่ 15 ก็ทำการเตรียมเบสที่ 10 M
* กรด คือ สาร เมื่อละลายน้ำแล้วแตกตัวให้ H+
* เบส คือ สาร เมื่อละลายน้ำแล้วแตกตัวให้ OH-
ในปกติ เราจะบอกความเป็นกรดเบสโดยอาศัยค่าความเข้มข้นของไฮโดรเนียมไอออน [H+] แต่มันไม่สะดวกในการอ้างถึงเพราะมันจะอยู่ในรูปของเลข 10 ยกกำลังที่มีเลขชี้กำลังติดลบนะคะ อย่าง เช่น 10^-7 ประมาณนี้ เขาจึงอาศัยคณิตศาสตร์เข้ามาช่วยให้ตัวเลขเหลือน้อยลง โดยใช้ลอการิทึม โดยมีสูตรว่า
pH = - log[H+]
จะทำให้ในการกล่าวถึงความเป็นกรดเบสทำได้ง่ายขึ้นนะคะ
อย่างเช่น ถ้า [H+] = 10^-7
pH = - log(10^-7) = - (-7) = 7 คะ
ตัวอย่าง pH ของน้ำ
เมื่อใส่ค่า p หรือ –log ลงทั้งสองข้าง ของสมการ
pH หรือ –log H+ ของน้ำ = -log (1 * 10^-7)
pH = -(log 1 + log 10^-7)
= -{log 1 + (-7 log 10)}
= -(log 1 – 7 log 10)
= -log 1 + 7 log 10
ตามหลักคณิตศาสตร์ log 1 มีค่าเท่ากับ 0 และ log 10 มีค่าเท่ากับ 1 (เครื่องหมายเพราะฉะนั้น) pH ของน้ำ = 0 + 7 = 7
จากการพิสูจน์ข้างต้นเมื่อน้ำมีค่า pH = 7 หรือมีค่า H+ 1 อะตอมจากน้ำทุกๆ 10^7 โมเลกุล ถ้าเราเอาน้ำอัดลมมาวัดค่า pH สมมุติวัดได้ค่า pH = 5 ซึ่งก็หมายความว่ามี H+ 1 อะตอมจากทั้งหมด 10^5 โมเลกุล ความเป็นกรดของน้ำอัดลม จึงมีค่าสูงกว่าน้ำธรรมดาถึง 100 เท่า
ค่า pH ส่วนใหญ่มีค่าอยู่ในช่วง 1-14 ครับ แต่สามารถน้อยกว่า 1 หรือมากกว่า 14 ก็ได้คะ
ตัวอย่าง 1
ถ้าเราต้องการเปลี่ยน pH 1 ที่มีความเข้มข้น 10-1 mol/L ให้เป็น pH 2 เราควรทำอย่างไร
ตามสูตร C1V1 = C2V2
เมื่อ C เป็นความเข้มข้น มีหน่วยเป็น โมลต่อลิตร
V เป็นปริมาตรหน่วยเป็น ลูกบาศก์เมตร (อาจใช้เป็นลิตร หรือลูกบาศก์เมตรก็ได้)
เช่น เอา pH1 มา 100 ลูกบาศก์เซนติเมตร จะได้
10-1*100 = 10-2*V2
0.1*100 = 0.01 * V2
V2 = 1000
คือต้องทำให้สารละลายมีปริมาตร 1000 ลูกบาศก์เซนติเมตรโดยการเติมน้ำลงไปอีก 900 ลูกบาศก์เซนติเมตรค่ะ นั่นหมายถึงการปรับพีเอชจาก 1 เป็น 2 นั้น ต้องเติมน้ำเข้าไปเพิ่มจากปริมาณเดิมถึง 9 เท่า
ทีนี้อยากถามสมาชิก Blog ว่าแล้วถ้าปรับพีเอชจาก 1 ซึ่งเป็นกรดให้มีค่าเป็นกลางพีเอชประมาณ 6 ต้องเติมน้ำเข้าไปเพิ่มอีกเท่าไรคะ ???
อ่านบทความทั้งหมด
จึงเป็น บทเรียนที่เราเรียนกันจนทุกวันนี้ คุ้นๆหูในนามของ นิยามกรด-เบส ของ อาเรเนียส ที่กล่าวไว้ว่า
กรด คือ สาร เมื่อละลายน้ำแล้วแตกตัวให้ H+
เบส คือ สาร เมื่อละลายน้ำแล้วแตกตัวให้ OH-
ค่า pH เป็นค่าที่ใช้บอกความแรงของกรดหรือเบสอย่างง่ายๆ นิยมใช้กันอย่างแพร่หลายกับผลิตภัณฑ์ทั่วไปไม่เฉพาะพวกสารเคมี คนทั่วไปเข้าใจได้ ค่าpHนี้กำหนดโดยความเข้มข้นของโปรตอน (H+) ในสารละลาย ยิ่งโปรตอนเข้มข้นมากซึ่งก็คือเป็นกรดมาก pHจะต่ำ ในทางกลับกันถ้าสารละลายเป็นเบส คือความเข้มข้นของโปรตอนต่ำ pH จะสูงค่าpH คำนวณได้จากสูตรนี้
pH = -log[H+]
โดย [H+] คือความเข้มข้นของโปรตอนในหน่วย โมล/ลิตร
โมล คือ หน่วยวัดปริมาตรทางเคมี โดยปกติอ้างอิงจากน้ำหนักจริงของสารหารด้วยน้ำหนักโมเลกุลของสารชนิดนั้น ซึ่งเป็นค่าคงที่
ในการวัดความเป็น กรด – เบส ในสารละลายนั้น เราใช้คำว่า “pH” เป็นตัวบ่งชี้ ตัว p ย่อมาจาคำว่า power ซึ่งมีความหมายในเชิงยกกำลัง ส่วน H นั้นหมายถึง ความเข้มของประจุไฮโดรเจน pH มีค่าเป็นตัวเลขตั้งแต่ 0 – 14 สารประกอบที่มีค่า pH 5 มีประจุไฮโดรเจนมากกว่า สารประกอบที่มีค่า pH 6 ถึง 10 เท่า
น้ำบริสุทธิ์มีค่า pH เป็นกลางอยู่ที่ pH 7 นั้นหมายถึง น้ำ 1 ลิตร ที่อุณหภูมิ 25 องศาเซลเซียส มีประจุไฮโดรเจน และประจุไฮดรอกไซด์ อยู่จำนวนเท่ากันคือ 1 x 10 –7 โมล
* เบสแก่ คือ เบสที่แตกตัวได้มากหรือ เบสที่แตกตัวได้ 100 % หรือเรียกอีกชื่อหนึ่งว่า
อิเล็กโทรไลต์แก่ ได้แก่ เบสหมู่ 1 ทุกตัว และเบสหมู่ 2 ยกเว้น Be(OH)2
* กรดแก่ คือ กรดที่แตกตัวได้มากหรือ เบสที่แตกตัวได้ 100 % หรือเรียกอีกชื่อหนึ่งว่า
อิเล็กโทรไลต์แก่ แบ่งออกเป็น
กรด Hydro ได้แก่ HCl , HBr , HI
กรด Oxy ได้แก่ H2SO4 , HNO3 , HClO3 , HClO4
ข้อสังเกต กรด Oxy ที่แก่ ให้นำจำนวนออกซิเจนลบกับจำนวน H+ ที่แตกตัวได้
ถ้าผลลัพธ์ตั้งแต่ 2 ขึ้นไปจะเป็นกรดแก่
ค่า pH ปกติมีค่าที่นิยมใช้กันคือ อยู่ระหว่า 0 - 14
โดยการวัดค่า pH นั้นที่ 0 วัดจากค่าความเข้มข้นของกรด HCl ที่ความเข้มข้น ที่ 1 M
pH ที่ 7 วัดจากค่าของน้ำ (Pure Water)
pH ที่ 14 วัดจากค่าความเข้มข้นของเบส NaOH ที่ความเข้มข้นที่ 1 M
ในกรณีที่เราต้องการค่า pH เป็น -1 ก็ทำการเตรียมกรดที่ 10 M แต่ถ้าต้องการวัดค่า pH ที่ 15 ก็ทำการเตรียมเบสที่ 10 M
* กรด คือ สาร เมื่อละลายน้ำแล้วแตกตัวให้ H+
* เบส คือ สาร เมื่อละลายน้ำแล้วแตกตัวให้ OH-
ในปกติ เราจะบอกความเป็นกรดเบสโดยอาศัยค่าความเข้มข้นของไฮโดรเนียมไอออน [H+] แต่มันไม่สะดวกในการอ้างถึงเพราะมันจะอยู่ในรูปของเลข 10 ยกกำลังที่มีเลขชี้กำลังติดลบนะคะ อย่าง เช่น 10^-7 ประมาณนี้ เขาจึงอาศัยคณิตศาสตร์เข้ามาช่วยให้ตัวเลขเหลือน้อยลง โดยใช้ลอการิทึม โดยมีสูตรว่า
pH = - log[H+]
จะทำให้ในการกล่าวถึงความเป็นกรดเบสทำได้ง่ายขึ้นนะคะ
อย่างเช่น ถ้า [H+] = 10^-7
pH = - log(10^-7) = - (-7) = 7 คะ
ตัวอย่าง pH ของน้ำ
เมื่อใส่ค่า p หรือ –log ลงทั้งสองข้าง ของสมการ
pH หรือ –log H+ ของน้ำ = -log (1 * 10^-7)
pH = -(log 1 + log 10^-7)
= -{log 1 + (-7 log 10)}
= -(log 1 – 7 log 10)
= -log 1 + 7 log 10
ตามหลักคณิตศาสตร์ log 1 มีค่าเท่ากับ 0 และ log 10 มีค่าเท่ากับ 1 (เครื่องหมายเพราะฉะนั้น) pH ของน้ำ = 0 + 7 = 7
จากการพิสูจน์ข้างต้นเมื่อน้ำมีค่า pH = 7 หรือมีค่า H+ 1 อะตอมจากน้ำทุกๆ 10^7 โมเลกุล ถ้าเราเอาน้ำอัดลมมาวัดค่า pH สมมุติวัดได้ค่า pH = 5 ซึ่งก็หมายความว่ามี H+ 1 อะตอมจากทั้งหมด 10^5 โมเลกุล ความเป็นกรดของน้ำอัดลม จึงมีค่าสูงกว่าน้ำธรรมดาถึง 100 เท่า
ค่า pH ส่วนใหญ่มีค่าอยู่ในช่วง 1-14 ครับ แต่สามารถน้อยกว่า 1 หรือมากกว่า 14 ก็ได้คะ
ตัวอย่าง 1
ถ้าเราต้องการเปลี่ยน pH 1 ที่มีความเข้มข้น 10-1 mol/L ให้เป็น pH 2 เราควรทำอย่างไร
ตามสูตร C1V1 = C2V2
เมื่อ C เป็นความเข้มข้น มีหน่วยเป็น โมลต่อลิตร
V เป็นปริมาตรหน่วยเป็น ลูกบาศก์เมตร (อาจใช้เป็นลิตร หรือลูกบาศก์เมตรก็ได้)
เช่น เอา pH1 มา 100 ลูกบาศก์เซนติเมตร จะได้
10-1*100 = 10-2*V2
0.1*100 = 0.01 * V2
V2 = 1000
คือต้องทำให้สารละลายมีปริมาตร 1000 ลูกบาศก์เซนติเมตรโดยการเติมน้ำลงไปอีก 900 ลูกบาศก์เซนติเมตรค่ะ นั่นหมายถึงการปรับพีเอชจาก 1 เป็น 2 นั้น ต้องเติมน้ำเข้าไปเพิ่มจากปริมาณเดิมถึง 9 เท่า
ทีนี้อยากถามสมาชิก Blog ว่าแล้วถ้าปรับพีเอชจาก 1 ซึ่งเป็นกรดให้มีค่าเป็นกลางพีเอชประมาณ 6 ต้องเติมน้ำเข้าไปเพิ่มอีกเท่าไรคะ ???